- Autor Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:40.
- Zadnja promjena 2025-06-01 07:36.
Ključna razlika između reakcija prvog i drugog reda je ta što brzina reakcija prvog reda ovisi o prvoj potenciji koncentracije reaktanta u jednadžbi brzine, dok brzina reakcija drugog reda ovisi o drugoj potenciji koncentracije izraz u jednadžbi stope.
Red reakcije je zbroj stupnjeva do kojih se podižu koncentracije reaktanata u jednadžbi zakona brzine. Postoji nekoliko oblika reakcija prema ovoj definiciji; reakcije nultog reda (ove reakcije ne ovise o koncentraciji reaktanata), reakcije prvog reda i reakcije drugog reda.
Što su reakcije prve narudžbe?
Reakcije prvog reda su kemijske reakcije čija brzina reakcije ovisi o molarnoj koncentraciji jednog od reaktanata koji sudjeluju u reakciji. Prema tome, prema gornjoj definiciji za redoslijed reakcije, zbroj stupnjeva do kojih se povećavaju koncentracije reaktanata u jednadžbi zakona o brzini uvijek će biti 1. Može postojati ili jedan reaktant koji sudjeluje u tim reakcijama. Tada koncentracija tog reaktanta određuje brzinu reakcije. Ali ponekad postoji više od jednog reaktanta koji sudjeluje u tim reakcijama, tada će jedan od tih reaktanata odrediti brzinu reakcije.
Razmotrimo primjer kako bismo razumjeli ovaj koncept. U reakciji razgradnje N2O5, nastaje NO2 i O 2 plinovi kao proizvodi. Budući da ima samo jedan reaktant, reakciju i jednadžbu brzine možemo napisati na sljedeći način.
2N2O5(g) → 4NO2(g) + O 2(g)
Stopa=k[N2O5(g)]m
Ovdje je k konstanta brzine za ovu reakciju, a m je redoslijed reakcije. Prema tome, iz eksperimentalnih određivanja, vrijednost m je 1. Dakle, ovo je reakcija prvog reda.
Što su reakcije drugog reda?
Reakcije drugog reda su kemijske reakcije čija brzina reakcije ovisi o molarnoj koncentraciji dvaju reaktanata ili drugoj potenciji jednog reaktanta koji je uključen u reakciju. Prema tome, prema gornjoj definiciji za redoslijed reakcije, zbroj potencija do kojih se podižu koncentracije reaktanata u jednadžbi zakona brzine uvijek će biti 2. Ako postoje dva reaktanta, brzina reakcije ovisit će o prvoj potenciji koncentracije svakog reaktanta.
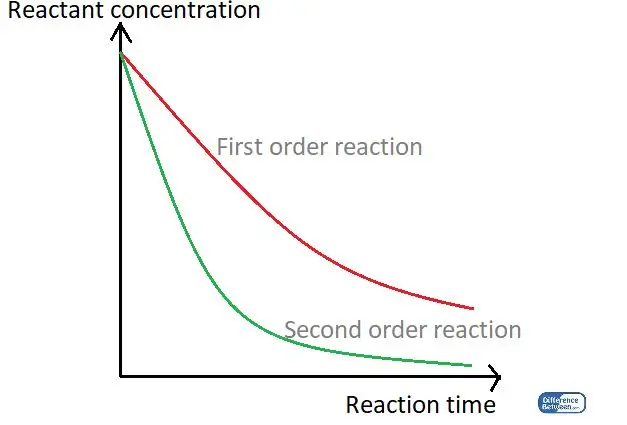
Slika 01: Grafikon koji uspoređuje dvije vrste redoslijeda reakcije koristeći njihovo vrijeme reakcije i koncentraciju reaktanta.
Ako koncentraciju reaktanta povećamo 2 puta (ako postoje dva reaktanta u jednadžbi brzine), tada se brzina reakcije poveća 4 puta. Na primjer, razmotrimo sljedeću reakciju.
2A → P
Ovdje je A reaktant, a P produkt. Zatim, ako je ovo reakcija drugog reda, jednadžba brzine za ovu reakciju je sljedeća.
Ocjena=k[A]2
Ali za reakciju s dva različita reaktanta kao što slijedi;
A + B → P
Ocjena=k[A]1[B]1
Koja je razlika između reakcija prvog i drugog reda?
Reakcije prvog reda su kemijske reakcije čija brzina reakcije ovisi o molarnoj koncentraciji jednog od reaktanata koji sudjeluju u reakciji. Dakle, ako povećamo koncentraciju reaktanta za 2 puta, brzina reakcije se povećava za 2 puta. Reakcije drugog reda su kemijske reakcije čija brzina reakcije ovisi o molarnoj koncentraciji dvaju reaktanata ili drugoj potenciji jednog reaktanta koji je uključen u reakciju. Dakle, ako povećamo koncentraciju reaktanta za 2 puta, brzina reakcije se povećava za 4 puta. Donja infografika prikazuje razliku između reakcija prvog i drugog reda u tabelarnom obliku.

Sažetak - Reakcije prvog naspram drugog reda
Postoje tri glavne vrste reakcija prema redoslijedu reakcije; reakcije nultog, prvog i drugog reda. Ključna razlika između reakcija prvog i drugog reda je u tome što brzina reakcije prvog reda ovisi o prvoj potenciji koncentracije reaktanta u jednadžbi brzine, dok brzina reakcije drugog reda ovisi o drugoj potenciji koncentracijskog člana u jednadžba stope.






