- Autor Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:40.
- Zadnja promjena 2025-06-01 07:36.
Ključna razlika - metan naspram etana
Metan i etan su najmanji članovi obitelji alkana. Molekulske formule ova dva organska spoja su CH4 i C2H6 redom. Ključna razlika između metana i etana je njihova kemijska struktura; Molekula etana može se smatrati dvjema metilnim skupinama spojenim kao dimer metilnih skupina. Ostale kemijske i fizikalne razlike uglavnom nastaju zbog ove strukturne razlike.
Što je metan?
Metan je najmanji član obitelji alkana s kemijskom formulom CH4(četiri atoma vodika vezana su na jedan atom ugljika). Smatra se glavnom komponentom prirodnog plina. Metan je plin bez boje, mirisa i okusa; također poznat kao karban, močvarni plin, prirodni plin, ugljikov tetrahidrid i vodikov karbid. Lako se zapali, a njegova je para lakša od zraka.
Metan se prirodno nalazi pod zemljom i ispod morskog dna. Atmosferski metan se smatra stakleničkim plinom. Metan se razgrađuje u CH3- s vodom u atmosferi.
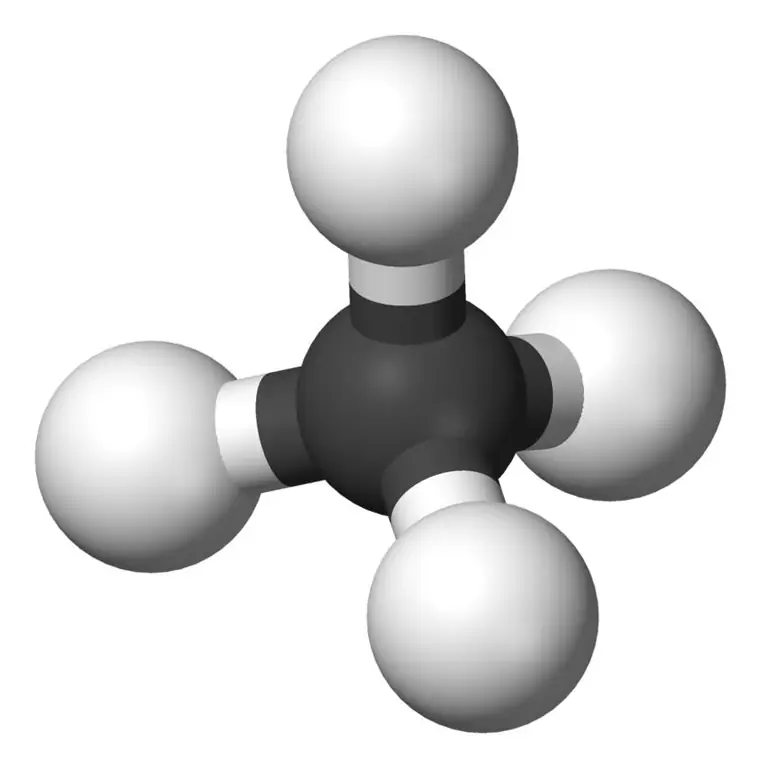
Što je Ethane?
Etan je plinoviti spoj bez boje i mirisa pri standardnoj temperaturi i tlaku. Njegova molekularna formula i molekularna težina su C2H6 odnosno 30,07 g·mol−1. Izolira se iz prirodnog plina, kao nusprodukt procesa rafiniranja nafte. Etan je vrlo važan u proizvodnji etilena.
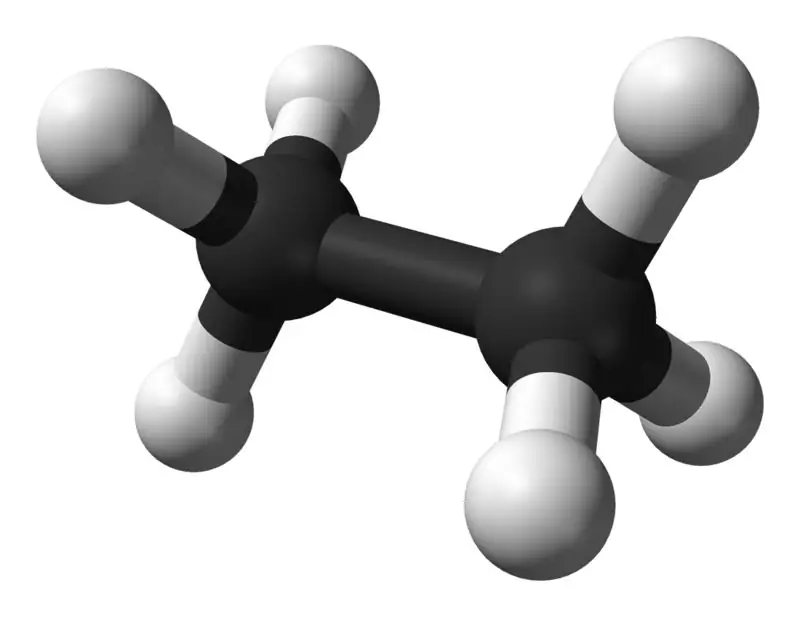
Koja je razlika između metana i etana?
Karakteristike metana i etana
Struktura:
Metan: Molekulska formula metana je CH4, i to je primjer tetraedarske molekule s četiri ekvivalentne C-H veze (sigma veze). Kut veze između H-C-H atoma je 109,50 i sve C-H veze su ekvivalentne, te je jednak 108,70 pm.
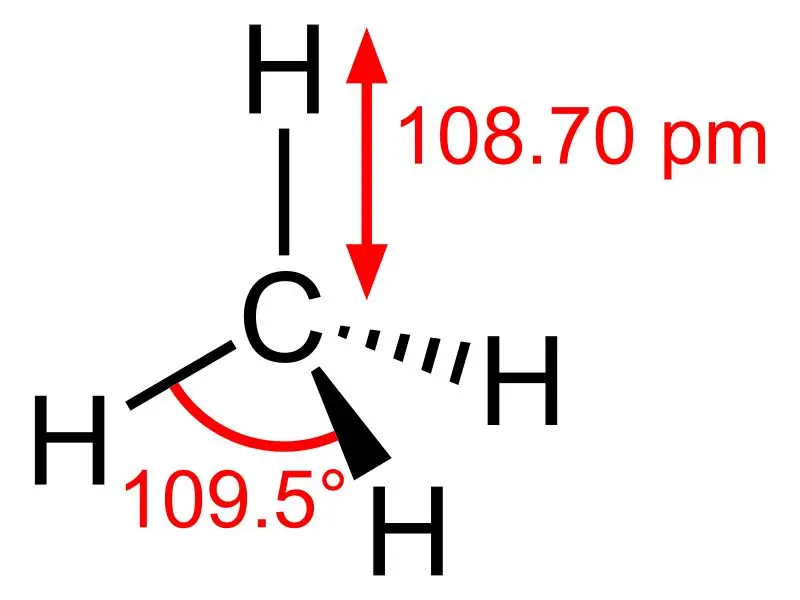
Etan: Molekulska formula etana je C2H6,i on je zasićeni ugljikovodik jer ne sadrži višestruke veze.
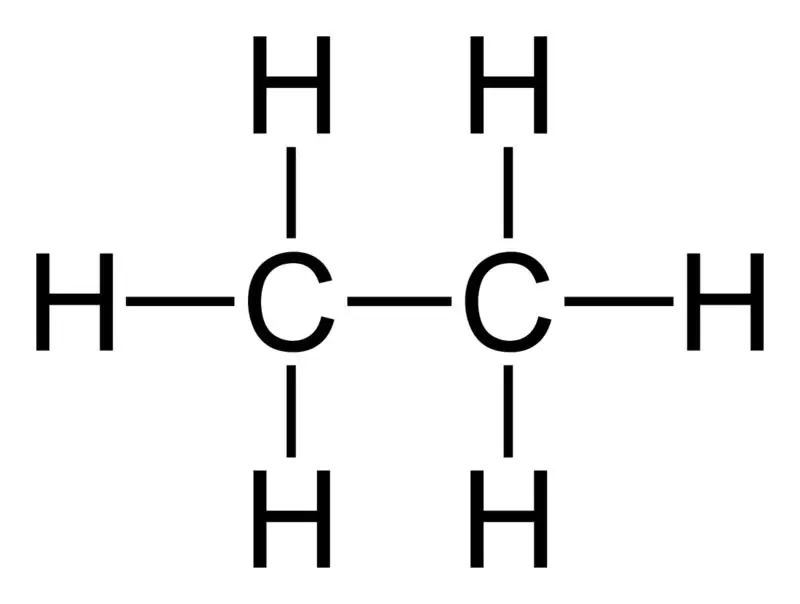
Kemijska svojstva:
Metan:
Stabilnost: Metan je kemijski vrlo stabilna molekula koja ne reagira s KMnO4, K2Cr 2O7, H2SO4 ili HNO 3 pod normalnim uvjetima.
Izgaranje: U prisutnosti viška zraka ili kisika, metan gori blijedoplavim nesvjetlećim plamenom stvarajući ugljični dioksid i vodu. To je vrlo egzotermna reakcija; stoga se koristi kao izvrsno gorivo. U prisutnosti nedovoljne količine zraka ili kisika, djelomično izgara u plin ugljični monoksid (CO).
Reakcije supstitucije: metan pokazuje reakcije supstitucije s halogenima. U tim reakcijama jedan ili više atoma vodika zamijenjeno je jednakim brojem atoma halogena i to se naziva "halogeniranje".” Reagira s klorom (Cl) i bromom (Br) u prisutnosti sunčeve svjetlosti.
Reakcija s parom: Kada se smjesa metana i pare propusti kroz zagrijani (1000 K) nikl oslonjen na površinu glinice, može proizvesti vodik.
Piroliza: Kada se metan zagrije na oko 1300 K, razgrađuje se na čađu i vodik.
Ethane:
Reakcije: Plin etan (CH3CH3) reagira s parama broma u prisutnosti svjetla da nastane bromoetan, (CH 3CH2Br) i vodikov bromid (HBr). To je supstitucijska reakcija; atom vodika u etanu je supstituiran atomom broma.
CH3CH3 + Br2 à CH3 CH2Br + HBr
Izgaranje: Potpuno izgaranje etana proizvodi 1559,7 kJ/mol (51,9 kJ/g) topline, ugljičnog dioksida i vode.
2 C2H6 + 7 O2 → 4 CO 2 + 6 H2O + 3120 kJ
Može se dogoditi i bez viška kisika, stvarajući mješavinu amorfnog ugljika i ugljikovog monoksida.
2 C2H6 + 3 O2 → 4 C + 6 H 2O + energija
2 C2H6 + 5 O2 → 4 CO + 6 H 2O + energija
2 C2H6 + 4 O2 → 2 C + 2 CO + 6 H2O + energija itd.
Definicije:
Reakcije supstitucije: Reakcija supstitucije je kemijska reakcija koja uključuje premještanje jedne funkcionalne skupine u kemijskom spoju i njezinu zamjenu drugom funkcionalnom skupinom.
Koristi:
Metan: Metan se koristi u mnogim industrijskim kemijskim procesima (kao gorivo, prirodni plin, ukapljeni prirodni plin) i transportira se kao rashlađeni fluid.
Etan: Etan se koristi kao gorivo za motore i kao rashladno sredstvo za sustave s ekstremno niskom temperaturom. Otprema se u čeličnim cilindrima kao ukapljeni plin pod vlastitim tlakom pare.






